"Wes' Brot ich ess, des' Lied ich sing'" - so möchte man etwas volkstümlich den Hintergrund der aktuellen WHO-Empfehlungen zur Klassifikation möglicher Impfstoff-Nebenwirkungen beschreiben...
Zum Hintergrund - Die Zulassung von Arzneimitteln und Impfstoffen
Da Impfungen als Maßnahmen der Prävention per defintionem an Gesunden vorgenommen werden und dies in der Regel millionenfach, ist bei ihnen der Anspruch an die Sicherheit dieser Medikamente besonders hoch - umso wichtiger ist es, mögliche Unerwünschte Arznei-Wirkungen (UAWs - vulgo: Nebenwirkungen) qualitativ und quantitativ zuverlässig zu erfassen, denn nur mit dieser Erfassung ist die unerlässliche Abwägung zwischen Nutzen und Risiko einer Impfung oder gar einer Impfstrategie überhaupt möglich.
Dass diese Vorgehensweise zur Gewährleistung der Arzneimittelsicherheit - die in den meisten westlichen Ländern ähnlich verläuft - vorsichtig formuliert nicht immer die Sicherheit bietet, die im Sinne des jeweiligen Patienten ist, hat in den letzten Jahren auch die Laien-Presse erreicht (Übersicht s. z.B. Handelsblatt 2018 - Übersichtsgraphik hier, ARD 2018, Gøtzsche 2015).
Erfassung von UAWs vor der Zulassung eines Arzneimittels/Impfstoffs - Zulassungsstudien
Die Erfassung möglicher UAWs beginnt naturgemäß schon während des Zulassungsprozesses eines Arzneimittels, der in Deutschland in mehreren Phasen verschiedener klinischer Prüfungen am Menschen abläuft. Phase I - III verlaufen (erst an gesunden Freiwilligen, dann an erst kleineren, dann größeren Gruppen "echter" Patienten) vor der behördlichen Zulassung; die Phase IV liegt nach der Zulassung, sie beschreibt die Überwachung eines neuen Arzneimittels nach der Markteinführung (so genannte Pharmakovigilanz - heutzutage: post-marketing-surveillance) (SMC 2017, BfArM 2013, DAZ 2012). Grundsätzlich werden die Ergebnisse dieser klinischen Prüfungen in Deutschland (PharmNet.Bund 2018) und auch in der EU veröffentlicht (EU 2018).
Diese klinischen Prüfungen bestehen in der Regel aus dem Vergleich zweier Studiengruppen: derjenigen, die das Prüfmedikament (Verumgruppe) und derjenigen, die ein wirkstofffreies Medikament, ein Placebo, erhält (Kontrollgruppe). Sie dienen zum einen dem Nachweis der Wirksamkeit der geprüften Substanz, zum anderen aber auch dem Aufdecken von UAWs durch den Vergleich der Häufigkeit gewünschter und eben auch unerwünschter Effekte in beiden Gruppen - dies gelingt aber naturgemäß unterschiedlich gut: "Die Wirksamkeit eines Arzneimittels lässt sich in kontrollierten Studien, die zu einer Zulassung führen sollen, relativ gut definieren. Das mit einem Arzneimittel einhergehende Risiko ist hingegen meist nur unzureichend bekannt. […] Gründe hierfür liegen in der statistischen Aussagekraft und in der speziellen Patientenselektion im Rahmen klinischer Prüfungen, die nicht unbedingt repräsentativ für das zukünftig zu behandelnde Kollektiv sein müssen." (BfArM 2010). Je seltener eine UAW auftritt, umso größer muss die Zahl der Studienteilnehmer sein, damit sie zuverlässig vor der Zulassung entdeckt wird (Röhrig 2010). Um z.B. aufzudecken, dass eine Gesundheitsstörung, die in der Kontrollgruppe einen von eintausend Teilnehmern beträfe unter dem Prüfmedikament doppelt so häufig auftritt, bräuchte es schon Studiengrößen von fast 40.000 Probanden/Patienten):
(Notwendige Studiengruppe, um einen zweifachen Anstieg einer UAW in der Verumgruppe bei einer kontrollierten oder Kohortenstudie erkennen zu können - BfArM 2010)
Studiengrößen dieser Dimension werden in Phase I - III und damit vor der Zulassung eines neuen Medikamentes praktisch nie erreicht; die Mehrzahl der klinischen Studien bewegen sich im Bereich von "im Durchschnitt 1.500; bei seltenen Erkrankungen teilweise nur 50-100" (BfArM 2010) Teilnehmern...
Das deutsche Bundesinstitut für Arzneimittel und Medizinprodukte schreibt in einer gemeinsam mit dem (in Deutschland für die Sicherheit der Impfstoff zuständigen) Paul-Ehrlich-Institut herausgegebenen Übersichtsarbeit dementsprechend [Hervorhebung von mir]: "Seltene und sehr seltene Nebenwirkungen (< 1%) lassen sich statistisch kaum belegen und können deshalb auch keinen beziehungsweise nicht adäquat Eingang in die Fach- und Gebrauchsinformationen zum Zeitpunkt der Zulassung finden. Deshalb kommt allen Aktivitäten nach erfolgter Marktzulassung, wie dem Erkennen und Verstehen von Arzneimittelrisiken, ihrer Bewertung und der Einleitung von Maßnahmen zu ihrer Minderung - der sogenannten Pharmakovigilanz - ein sehr hoher Stellenwert zu." (BfArM 2010).
Besonderheiten bei der Zulassung von Impfstoffen
Die qualitative und quantitative Beurteilung von UAWs von Impfstoffen (so genannen AEFIs - Adverse Events following Immunization) im Rahmen klinischer Prüfungen vor der Zulassung wird zusätzlich noch dadurch erschwert, dass Phase I - III-Studien bei Impfstoffen anders als bei allen anderen Medikamenten in aller Regel mit Kontrollgruppen durchgeführt werden, die kein Placebo erhalten, sondern einen anderen Impfstoff. Damit sind Auftreten und Häufigkeit von UAWs natürlich immer nur im Vergleich der beiden Impfstoffe, nicht aber im Vergleich zu einer wirklich ungeimpften Kontrollgruppe erfasst. Begründet wird dies damit, dass es ethisch nicht vertretbar sei, der Kontrollgruppe den Nutzen von Impfungen vorzuenthalten. Die WHO lässt in einem Expertenpapier zu diesem Thema placebokontrollierte Impfstoffstudien nur in sehr wenigen, sehr eingeschränkten Fällen zu (Rid 2014, WHO 2013).
Dieses Argument entbehrt nicht einer gewissen Bigotterie: auch bei allen anderen Medikamentenzulassungen (bei denen Placebo-kontrollierte Studien Vorschrift sind) enthalten die Zulassungsstudien Menschen mit einem real existierenden (nicht wie bei Impfungen: möglichen) Leidensdruck potentielle Linderung, Besserung oder Heilung ihrer Beschwerden durch die Placebogabe vor; denn spätestens Phase II und III finden ja an Patienten statt.
Erfassung von UAWs nach der Zulassung eines Arzneimittels/Impfstoffs - Pharmakovigilanz
Um Gesundheitsstörungen, die unter oder nach der Verabreichung eines zugelassenen Arzneimittels/Impfstoffs nach der Zulassung (und damit unter weniger kontrollierten Bedingungen) diesem Arzneimittel zuordnen zu können, bedarf es klarer Kriterien, wann von einem ursächlichen Zusammenhang zwischen Gesundheitsstörung und Verabreichung ausgegangen werden muss bzw. kann und wann dieser eher unwahrscheinlich ist oder gar ausgeschlossen werden kann.
Durchgesetzt hat sich hierfür (mit geringen Abwichungen) international (Edwards 2000) ein klares Schema, das z.B. auch von der WHO in ihrem eigenen Upsala Monitoring Center (UMC) für Arzneisicherheit(WHO/UMC 2018) und der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ 2005) verwendet wird und das bezüglich des Zusammenhangs unterscheidet zwischen sicher/wahrscheinlich/möglich/unwahrscheinlich/unklassifiziert/nicht beurteilbar. Eine Klassifikation als: sicher ausgeschlossen - fehlt.
(BfArM/PEI 2014)
AEFI und die WHO
Für die Erfassung von Impfstoff-UAWs verwendete die WHO bis zum Jahr 2013 eine Klassifikation, die sie selber expressis verbis an ihr eigenes UMC-Schema anlehnte - an der Formulierung wirkte wesentlich die mit Impfthemen befasste Brighton-Collaboration mit, daher firmieren diese Kriterien auch als "Brighton-Classification" (Puliyel 2018):
(WHO 2002 und 2005)
Im Jahr 2010 wurden diese Kriterien unter der Schirmherrschaft der WHO und dem "Council for International Organizations of Medical Sciences (CIOMS)" überarbeitet - von einer Arbeitsgruppe, in der von 40 Mitgliedern 19 Mitarbeiter der großen Impfstoffhersteller waren (CIOMS 2012, S. 143 ff. - von den anderen Mitgliedern fehlen Erklärungen zu eventuellen Interessenkonflikten).
Die entscheidende und weitestreichende Veränderung in der Bewertung von AEFIs ist, dass - erstmals und weltweit beispiellos in Pharmakovigilanz-Systemen - die offizielle Bewertungskategorie "Not a case of [AEFI]" eingeführt wurde; wo also andere Klassifikationen einschließlich der WHO-eigenen seitens des Upsala Monitioring Centers UMC der unvermeidlichen Restunsicherheit bei der Beurteilung medizinischer Ursache-Wirkungs-Zusammenhänge Rechnung trägt, indem ein gemeldeter Verdachtsfall schwächstenfalls als "unwahrscheinlich/unlikely" eingestuft wurde, sortiert die WHO bei Impfstoffen hier jetzt wesentlich radikaler.
Die Tragweite dieser scheinbar kleinen Änderung kann kaum überschätzt werden, weil damit ein solcher Verdachtsfall auch für zukünftige Betrachtungen ignoriert werden kann und wird - ein eventuell weiterer, gleich gelagerter Fall wäre dann nicht der zweite, sondern wieder ein Einzelfall, denn der erste ist ja klar aussortiert. Die Funktion der Pharmakovigilanz, aus eventuellen Wiederholungen oder gar Häufungen solcher Einzelfälle Risikosignale zu generieren, die dann in Studien gezielt untersucht werden könnten, wird so ad absurdum geführt.
Des weiteren werden AEFIs zukünftig über "case definitions" klassifiziert, Falldefinitionen, die Kriterien festlegen, nach denen eine UAW erfasst wird. So sinnvoll eine gewisse Standardisierung bei Erfassungssystemen sein kann, hier scheinen diese Falldefinitionen vor allem einem Zweck zu dienen: "If there is adequate evidence that an event does not meet a case definition, such an event should be rejected and should be reported as “Not a case of [AEFI]” (CIOMS 2012) - es geht also vor allem darum, Verdachtsfälle dieser hochproblematischen, neuen und beispiellosen Rubrik zuzuordnen.
Je komplexer und détailierter diese Falldefinitionen sind, desto leichter fällt naturgemäß das Aussortieren von Verdachtsfällen nach der zitierten Handlungsanweisung, da in diesen vor allem auch Ausschlusskriterien formuliert werden, wann ein Verdachtsfall eben nicht der Falldefinition entspricht. Der Verdacht, dass es auch gerade darum geht, Verdachtsfälle zu "zurückzuweisen" (das verwendete Verb reject hat noch ganz andere, negativere Konnotate...) wird erhärtet, wenn z.B. die case definition für etwas so banales wie einen Schmerz an der Einstichstelle zwanzig (!) Seiten umfasst (Gidudu 2012). Die Aufgabe der Pharmakovigilanz ist es jedoch nicht, zurückzuweisen, sondern ergebnisoffen Daten zu sammeln, um Risikosignale rechtzeitig zu erkennen (BfArM 2010). "Signal detection is no longer possible once AEFIs are removed from the system after being designated as ‘Not a case of [AEFI]’." (Puliyel 2018).
Einen besonderen haut-goût bekommen diese Falldefinitionen jedoch vor allem dadurch, dass an zahlreichen entsprechenden Veröffentlichungen von case definitions Impfstoffhersteller wie GSK, Sanofi oder Novartis mitarbeiteten - dies gilt für die erwähnte Definition von "Immunization site pain" (Gidudu 2012) genauso, wie für die von "Neonatal infection" (Vergnano 2016) oder "Neonatal death" (Pathirana 2016). Nicht, dass es nicht bisher schon ohne Falldefinition der WHO möglich gewesen wäre, diese Diagnosen zu stellen: hier definieren die Impfstoffhersteller hochoffiziell (!) die Kriterien mit, nach denen die Sicherheit ihrer Produkte in der Pharmakovigilanz überprüft werden... . Ein ebenfalls beispielloses Vorgehen.
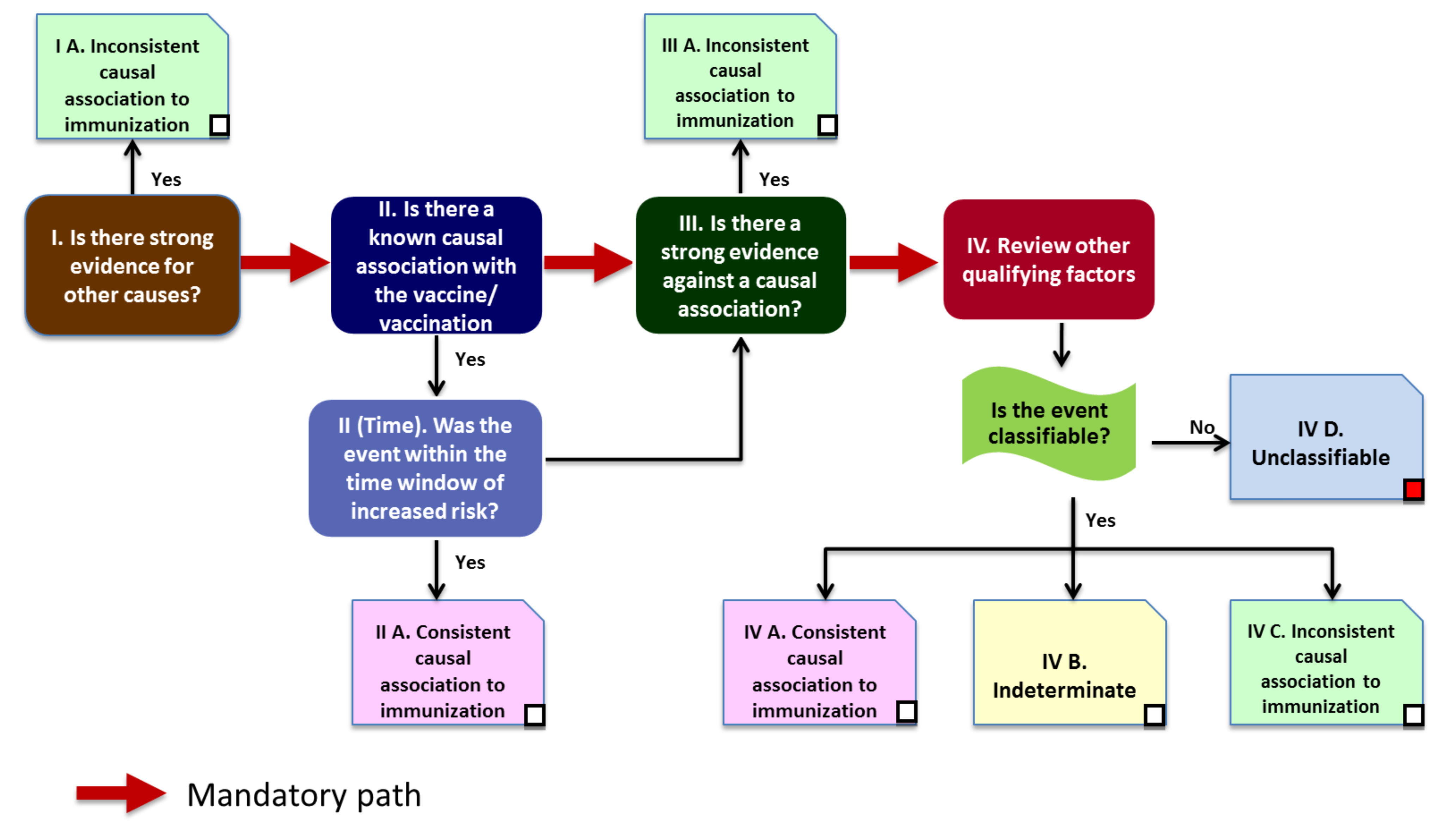
Für das konkrete Abwägen eines möglicherweise ursächlichen Zusammenhangs gibt die WHO seit 2013 das folgende Flussdiagramm vor:
(WHO 2018)
Schon die erste "Weggabelung" ist wissenschaftlich nicht haltbar, setzt sie doch ein in der Medizin eher seltenes, monokausales Verhältnis zwischen einer Ursache und einer Folge voraus. Die ignoriert zum einen die Tatsache, dass in biologischen Systemen für einen beobachteten Effekt oft mehrere Ursachen möglich sind, die für sich allein alle zum gleichen Ziel führen. Zum anderen und vor allem aber den wesentlich häufigeren Fall, dass für ein gesundheitliches Problem eine Kette mehrerer Faktoren eine Rolle spielt (z.B. eine Vorerkrankung, eine genetische Prädisposition, ...), von denen dann die Impfung "nur" der letztendlich auslösende war, wäre hiermit nicht zu erfassen. Die Impfung wäre durch dieses Vorgehen z.B. bei einem Kind mit einer genetischen Prädisposition, das einen Krampfanfall nach einer Sechsfachimpfung bekommt genauso exkulpiert, wie bei einem Erwachsenen, dessen Herzschwäche sich durch das Fieber nach der Grippeimpfung lebensbedrohlich verschlechtert. Alle anderen gängigen Klassifikationssysteme halten einen Kausalzusammenhang auch bei vorliegen anderer (mit-)ursächlicher Faktoren durchaus noch für möglich/possible (auch das WHO-eigene UMC-Schema! s.o.), bei Impfungen wird dies von vorneherein verneint. Die Absurdität dieses Vorgehens wird deutlich, wenn man es auf das Erfassen von Krankheitskomplikationen überträgt: in der von der WHO propagierten Logik wäre z.B. das Kind, das 2015 in Berlin als Folge einer Maserninfektion verstarb, kein Maserntodesfall, denn es hatte eine schwere kardiale Vorerkrankung und damit "strong evidence for other causes" (s. dazu hier).
Diesem Umstand trug die WHO selber noch vor einigen Jahren Rechnung, indem sie 2001 im damaligen Übersichtspapier zur Klassifikation von AEFI schrieb: "When adverse events are attributable to a vaccine, it is important to determine whether there is a predisposed set of subjects (by age, population, genetic, immunological, environmental, ethnic, sociological or underlying disease conditions) for any particular reaction." - man beachte: attributable (zuzuschreiben), nicht attributed (zugeschrieben)... (WHO 2001).
Mittlerweile fordert die WHO in ihren Definitionen aber realitätsfern und unwissenschaftlich einen monokausalen Ursache-Wirkungszusammenhang und definiert diesen so: "Causal association: A cause-and-effect relationship between a causative factor and a disease with no other factors intervening in the process." (WHO 2018 - Hervorhebung von mir)
Der zweite Schritt führt dann zum endgültigen erkenntnistheroretischen salto mortale: nur vorher bekannte Nebenwirkungen werden ab hier weiter untersucht. Die WHO fordert in diesem Zusammenhang unter anderem zwei Dinge: zum ersten die "biologische Plausibilität" "... the association should be compatible with existing theory and knowledge related to how the vaccine works." (WHO 2018). Mit anderen Worten: nur, was wir kennen und erklären können, sind wir bereit wahrzunehmen (man stelle sich diesen Gedanken übertragen auf andere Wissenschaftsbereiche wie z.B. die Quantenphysik vor...).
2001 schätzte die WHO den Wert dieser biologischen Plausibilität und a priori-Erklärbarkeit noch wesentlich realistischer und damit vor allem: wissenschaftlicher ein, indem sie formulierte: "The requirement for biological plausibility should not unduly influence negatively a consideration of causality. Biological plausibility is a less robust criterion than the others described. If an adverse event does not fit into known facts and the preconceived understanding of the adverse event or the vaccine under consideration, it clearly does not necessarily follow that new or hitherto unexpected events are improbable. Biological plausibility is most helpful when it is positive; it is less so when negative." (WHO 2001 - Hervorhebung von mir).
Zum zweiten den existierenden epidemiologischen Beweis, dass die Impfung den jeweiligen AEFI überhaupt auslösen kann; findet sich dieser nicht (was bei seltenen AEFIs angesichts der oft kleinen Studiengrößen (s.o.) häufig der Fall ist), wird eine Kausalität für den in Frage stehenden Einzelfall von vorneherein ausgeschlossen: "A strong “no” at the population level is inconsistent with causality at the individual level." (WHO 2018). Spätestens hier kommt es zum klassischen Zirkelschluss: was nicht schon vorher bewiesen wurde und nicht schon im Vorneherein erklärt werden kann, wird nicht wahrgenommen oder weiter untersucht.
Diese Forderung nach einem Beweis in epidemiologischen Studien lässt auch völlig außer Acht, dass ein fehlender Nachweis in solchen Studien das Fehlen eines Zusammenhangs keineswegs ausschließt. Unter der Überschrift "Absence of evidence is not evidence of absence" schreiben Autoren der britischen Cochrane-Collaboration "When is it reasonable to claim that a study has proved that no effect or no difference exists? The correct answer is “never,” because some uncertainty will always exist. […] We need to create a culture that is comfortable with estimating and discussing uncertainty." (Alderson 2004) und als mögliche Erklärung "The sample size of controlled trials is generally inadequate […] The term "negative" should not be used in this context" (Altman 1995).
Auch dies wusste man bei der WHO 2001 noch sehr genau: "The clearest and most reliable way to determine whether an adverse event is causally related to vaccination is by comparing rates of the event in a vaccinated and non-vaccinated group in a randomized clinical trial. Such trials, however, can never be large enough to assess very rare events, and postmarketing surveillance systems are required to identify events potentially related to vaccination." (WHO 2001 - Hervorhebung von mir).
Das in diesem Schritt verwendet "time window of increased risk" zum Erfassen von AEFIs ist hochproblematisch, weil es, in der Regel willkürlich auf wenige Tage bis Wochen begrenzt, mögliche langfristige Folgen von Impfungen wie z.B. Multiple Sklerose (Hernán 2004) oder die auf der Aluminiumbelastung beruhende Makrophagische Myofasciitis (Rigolet 2014) als AEFI ignoriert.
Auch die im dritten Schritt untersuchte "strong evidence against a causal association" ist wissenschaftstheoretisch problematisch, worauf die renommierte Cochrane Collaboration in ihrer Veröffentllichung "An invisible unicorn has been grazing in my office for a month… Prove me wrong." (Burton 2016) hinweist - das Widerlegen wissenschaftlicher Annahmen ist aus den verschiedensten Gründen prinzipiell immer mit besonderen Schwierigkeiten verbunden... . "When we are told that "there is no evidence that A causes B" we should first ask whether absence of evidence means simply that there is no information at all. If there are data we whould look for quantification of the association rather than just a P value. Where risks are small P values may well mislead: confidence intervals are likely to be wide, indicating considerable uncertainty. While we can never prove the absence of a relation, when necessary we should seek evidence against the link between A and B - for example, from case-control studies. The importance of carrying out such studies will relate to the seriousness of the postulated effect an how widespread is the exposure in the population." (Altman 1995, Hervorhebungen von mir).
Zusammenfassend drängt sich bei der aktuellen WHO-Strategie zur Erfassung und Klassifikation von AEFIs der klare Verdacht auf, dass es nicht mehr darum geht, AEFI-Verdachtsfälle möglichst vollständig zu erfassen und ergebnisoffen auf ihren Zusammenhang mit der jeweiligen Impfung zu bewerten, sondern vielmehr darum, eventuelle Risikosignale möglichst schon im Keim zu ersticken, ihre Erfassung mit industrienahen Definitionen zu erschweren und ihre Bewertung wissenschaftlich unhaltbar so zu gestalten, dass ein ursächlicher Zusammenhang zwischen Nebenwirkung und Impfung in fast jedem Fall ausgeschlossen wird.
Dieses Vorgehen ist - trotz allem wissenschaftlichen Anstrich - letztlich nicht nur unwissenschaftlich, sondern auch ethisch hochproblematisch: es konterkariert die besonders hohen Sicherheitsansprüche, die gerade an präventiv eingesetzte Medikamente gestellt werden müssen und hebelt die auch von deutschen Arzneibehörden zu Recht als zentral angesehen Pharmakovigilanz nach erfolgter Zulassung in letzter Konsequenz aus. Es gibt überhaupt keine nachvollziehbaren Gründe, warum für Impfstoffe andere Regeln der Zulassung oder Pharmakovigilanz gelten sollten, als für alle anderen Medikamente - wenn überhaupt, dann müssten die Ansprüche höher, die Anforderungen schärfer sein, da es wenige andere Pharmaka gibt, die wie Impfstoffe regelhaft und flächendeckend beschwerdefreien, gesunden Menschen (vor allem Kindern) ohne jeden realen Leidensdruck verabreicht werden. Inwieweit die WHO-Vorgaben daher überhaupt mit z.B. deutschem und europäischem Arzneimittelrecht (das dem EU Prinzip des "Vorsorgeprinzips" verpflichtet ist) vereinbar sind, bleibt zu überprüfen.
Angesichts des allgegenwärtigen Lamentos über das sinkende Vertrauen in Impfungen, Impfempfehlungen und Impfstrategien wundern erkennbar industrienahe Vorgaben wie die hier untersuchten umso mehr: sie sind sicher nicht dazu angetan, verloren gegangenes Vertrauen in unabhängige Entscheidungen der WHO und damit auch anderer Impfkommissionen wieder herzustellen.
Die WHO erzeugt hier eine Fata morgana pharmakologischer Scheinsicherheit anstatt zuzugeben, wie viel wir über Impfungen, deren Wirkungen und Nebenwirkungen eben nicht wissen, an der Beseitigung dieses Nichtwissens konstruktiv mitzuwirken und damit das bejammerte fehlende Vertrauen der Bevölkerung in Impfempfehlungen zu restituieren. Sie untermauert einmal mehr den in den letzten Jahren zunehmend thematisierten Verdacht der fehlenden Unabhängigkeit und einer mit ihrer genuinen Aufgabe unvereinbaren Nähe zur Interessensgruppen wie z.B. der pharmazeutischen Industrie (z.B. durch ihre maßgebliche Finanzierung durch die Bill and Melinda Gates Foundation (arte 2017, ZEIT ONLINE 2017), die sich selber auch über Pharma-Aktien finanziert (arte 2017, Global Justice 2017).
Literatur
Alderson P. 2004. BMJ. 328:476–77
Altman DG. 1995. BMJ. 311:485
AKDÄ. 2005. Arzneiverordnung in der Praxis - Pharmakovigilanz.
ARD. 2018. Planet Wissen - Arzneimittel-Skandale. Abruf 22.07.2018
arte. 2017. Die WHO - Im Griff der Lobyisten? Abruf 26.07.2018
BfArM. 2013. Wie ein Arzneimittel entsteht. Abruf 22.07.2018
BfArM/PEI. 2014. Bulletin zur Arzneimittelsicherheit - Ausgabe 4/2014. Abruf 22.07.2018
BfArM/PEI. 2010. Bulletin zur Arzneimittelsicherheit - Ausgabe 1/2010. Abruf 22.07.2018
Burton M. 2016. An invisible unicorn has been grazing in my office for a month… Prove me wrong. Abruf 25.07.2018
CIOMS. 2012. Definition and Application of Terms for Vaccine Pharmacovigilance. Abruf 22.07.2018
DAZ. 2012. Vom Wirkstoff zum Arzneimittel. Abruf 22.07.2018
Edwards IR. 2000. The Lancet. 356(9237):1255–59
EU. 2018. Clincal Trials Register. Abruf 22.07.2018
Gidudu JF. 2012. Vaccine. 30(30):4558–77
Global Justice: Gated Development - Is the Gates Foundation always a force for good? Abruf 26.07.2018
Gøtzsche P. Tödliche Medizin und organisierte Kriminalität. München, 2015.
Hernan MA. 2004. Neurology. 63(5):838–42
Handelsblatt. 2018. Die größten Pharmaskandale unseres Jahrtausends. Abruf 22.07.2018
PharmNet.Bund. 2018. Klinische Prüfungen. Abruf 22.07.2018
Puliyel J. 2018. F1000Research. 7:243
Rid A. 2014. Vaccine. 32(37):4708–12
Rigolet M. 2014. Frontiers in Neurology. 5:
Röhrig B. 2010. Dtsch Arztebl Int. 107(31-32): 552-6
SMC/Science Media Center. 2017. Arzneimittel: Von der Entwicklung bis zur Zulassung. Abruf 22.07.2018
Vergnano S. 2016. Vaccine. 34(49):6038–46
WHO/UMC. 2018. The use of the WHO-UMC system for standardised case causality assessment. Abruf 22.07.2018
WHO. 2013. Expert consultation on the use of placebos in vaccine trials. Geneva: World Health Organization. Abruf 22.07.2018
WHO. 2018. Causality assessment of adverse events following immunization (AEFI). Geneva: World Health Organization.
WHO. 2005. Adverse Events Following Immunization (AEFI): Causality Assessment. Abruf 22.07.2005
WHO. 2002. Adverse Events Following Immunization: Causality assessment. Abruf 22.07.2018
WHO. 2001. Causality assessment of adverse events following immunization. WER 76, 85–92.
ZEIT ONLINE. 2017. WHO: Der heimliche WHO-Chef heißt Bill Gates. Abruf 26.07.2018